
Figura 1. Subtipos de síndrome cardio-renal (SCR) tipo 1. IC: insuficiencia cardíaca. ERC: enfermedad renal crónica.
ARTICULO DE REVISION (Versión en español)
Síndrome cardio-renal tipo 1
Mecanismos fisiopatológicos y papel de los nuevos biomarcadores
Sylvia Dávila Mora1, Eduardo Zea Dávila1, Eduardo Nani Silva2, Evandro Tinoco Mesquita3,
Wolney de Andrade Martins3, Humberto Villacorta Junior3
1 Médico especialista en Cardiología. Universidad Federal Fluminense (UFF). Niterói. RJ. Brasil.
2 Máster en Cardiología. Universidad Federal Fluminense (UFF). Profesor de la Facultad de Medicina.UFF. Niterói. RJ. Brasil.
2 Doctor en Cardiología. Universidad de São Paulo. Profesor de la Facultad de Medicina. Universidad Federal Fluminense (UFF). Niterói. RJ. Brasil.
Institución: Hospital Universitario Antonio Pedro. Universidad Federal Fluminense (UFF). Departamento de Medicina Clínica. Niterói (RJ). Brasil.
Correspondencia: Dra. Sylvia Dávila Mora.
Avenida Marques do Paraná 303, sexto piso, centro, Niterói, RJ, Brasil. CEP: 24030-215. Teléfono: +552126299207.
E-mail: silvi.davila.m@gmail.com
Recibido: 28/09/2015
Aceptado: 20/12/2015
Resumen
La alteración de la función renal en los pacientes con insuficiencia cardíaca descompensada es frecuente y está
asociada con alta morbimortalidad. El síndrome cardio-renal es un disturbio entre el corazón y el riñón, en donde
la alteración primaria de un órgano resulta en la disfunción secundaria y perjuicio del otro. La presente revisión
tiene como objetivo proveer una visión general del síndrome cardio-renal tipo 1, su fisiopatología y diagnóstico a
través de nuevos biomarcadores. El síndrome cardio-renal tipo 1 está presente en aproximadamente el 23-33% de
los pacientes internados con insuficiencia cardíaca descompensada. Se caracteriza por el desarrollo de rápida lesión
renal en pacientes con disfunción cardíaca aguda. Son múltiples los mecanismos involucrados en su patogénesis.
Cambios hemodinámicos llevan a congestión venosa, activación del sistema renina angiotensina aldosterona y del
sistema simpático, responsables de mayor sobrecarga de volumen y de la alteración de la función renal. Nuevos
biomarcadores como NGAL, KIM-1 están siendo evaluados para la detección precoz de lesión renal en pacientes
con insuficiencia cardíaca descompensada. El NGAL junto con el BNP, son probablemente los marcadores que
presentan mayor evidencia de éxito en el diagnostico del síndrome cardio-renal tipo 1, BNP aporta precozmente
datos de presencia de sobrecarga de volumen y NGAL indica lesión renal precoz. Un mejor entendimiento de los
mecanismos fisiopatológicos de este síndrome, permitirá encontrar estrategias que ayuden en la prevención de las
alteraciones renales en pacientes con insuficiencia cardíaca así como un tratamiento adecuado.
Palabras clave: Insuficiencia cardíaca; Lesión renal aguda; Síndrome cardio-renal
Introducción
La insuficiencia cardíaca (IC) es un síndrome sistémico
complejo, considerado un problema de salud pública
debido al aumento continuo de su prevalencia. Es una de
las principales causas de hospitalización, especialmente,
de casos de IC crónica descompensada1.
Las alteraciones cardíacas pueden causar efectos negativos
en la función renal, así como, la insuficiencia renal puede
comprometer la función cardíaca, iniciándose una compleja
combinación de mecanismos neurohumorales que
pueden perjudicar ambos órganos. Estas interacciones entre
corazón y riñón son conocidas como síndrome cardiorenal
(SCR)2,3. El síndrome cardio-renal es definido como un disturbio fisiopatológico del corazón y los riñones,
en el cual la disfunción aguda o crónica de un órgano
puede inducir disfunción aguda o crónica del otro4-6.
Años atrás se creía que la reducción del flujo renal era
el único mecanismo que explicaba la fisiopatología de
la lesión renal aguda; pero posteriormente, se evidenció que el flujo sanguíneo renal se mantiene preservado7 hasta que el índice cardíaco es menor a 1,5 L/m2. El
estudio ESCAPE (Evaluation Study of Congestive
Heart Failure And Pulmonary Artery Catheterization
Effectiveness) sugiere que la lesión renal asociada a
IC no es sólo una consecuencia del hipoflujo renal8.
Varias investigaciones han demostrado que las interacciones
cardio-renales ocurren bidireccionalmente y
con variedad de presentaciones9. Para tener un mejor
entendimiento de su fisiopatología, se lo clasifica en
cinco tipos:
- Tipo 1 o síndrome cardio-renal agudo: es el tipo más
frecuente y se caracteriza por un rápido deterioro de
la función cardíaca que lleva a lesión renal aguda.
- Tipo 2 o síndrome cardio-renal crónico: la disfunción
cardíaca ocasiona enfermedad renal crónica
progresiva (ERC). Aproximadamente el 50% de los
pacientes con IC crónica tienen ERC, cuya asociación
está relacionada con alta mortalidad.
- Tipo 3 o síndrome renocardíaco agudo: existe un
súbito deterioro de la función renal que ocasiona
disfunción cardíaca aguda (arritmias, IC o isquemia).
- Tipo 4 o síndrome renocardíaco crónico: ERC
que contribuye a disfunción sistólica y diastólica,
hipertrofia ventricular e incremento de eventos cardiovasculares
adversos.
- Tipo 5 o síndrome cardio-renal secundario: enfermedades
sistémicas agudas o crónicas (sepsis, diabetes
mellitus) causan disfunción cardíaca y renal.
Esta clasificación no es estática, de tal forma que un
paciente con IC crónica y enfermedad renal crónica,
considerado como SCR tipo 2, puede tener un episodio
agudo de descompensación cardíaca con evolución hacia
una lesión renal aguda que requiera internación y por lo
tanto sea considerado como SCR tipo 13.
La alteración de la función renal es identificada como
el mayor predictor de mortalidad de los pacientes con
IC descompensada, siendo incluso mejor que la clase
funcional de New York Heart Association (NYHA) y la
fracción de eyección de ventrículo izquierdo (FEVI). Por
este motivo es indispensable que durante el tratamiento
de la IC se mantenga una adecuada función renal2.
Debido al impacto que el SCR agudo tiene en la morbimortalidad
de los pacientes, es fundamental tener un
adecuado conocimiento de los mecanismos fisiopatológicos
involucrados, por lo cual la presente revisión
bibliográfica tiene como objetivo principal proporcionar
evidencias recientes que ayuden a un mejor entendimiento
de esta patología; así como también, dar a
conocer los nuevos biomarcadores que pueden ayudar
en la detección precoz de lesión renal aguda.
Síndrome cardio-renal tipo 1
Características
El síndrome cardio-renal tipo 1 se caracteriza por el rápido
desarrollo de lesión renal debido a una disfunción
cardíaca aguda, como por ejemplo insuficiencia cardíaca
descompensada, síndromes coronarios agudos, shock
cardiogénico o pos-operatorio de cirugía cardíaca10. Se
divide en 4 subtipos (Figura 1).

Figura 1. Subtipos de síndrome cardio-renal (SCR) tipo 1. IC: insuficiencia cardíaca. ERC: enfermedad renal crónica.
La disfunción renal es un hallazgo frecuente en los
pacientes con IC, siendo considerada como un factor
independiente de mal pronóstico. En el estudio Acute
Decompensated Heart Failure National Registry (ADHERE)11, se encontró que sólo un 9% de los 118465
pacientes internados con IC aguda presentó función renal
normal, y se reportó disfunción moderada a grave en el
30-35% dos casos.
La IC descompensada es la causa más común de SCR
tipo1, con una prevalencia de 23-33%12, la mayor proporción
de casos ocurre en los primeros 3-5 días de
internación hospitalaria13,14. Además, puede presentarse
en pacientes con enfermedad renal preexistente, los
cuales tienen un 60% de predisposición para desarrollar
un cuadro renal agudo. El incremento de los niveles de
creatinina de 0,3 mg/dL15,16 o el aumento de 25-50% de los
niveles de creatinina basal han sido utilizados para definir
al SCR tipo 116. Diferencias en las definiciones usadas en
los estudios pueden alterar la estimativa epidemiológica
de este síndrome4. Niveles de urea nitrogenada en sangre
mayores a 50 mg/dL fueron encontrados en el 20% de los
pacientes con SCR agudo15 y en el estudio ADHERE11
fueron considerados como fuerte predictor de mortalidad
intrahospitalaria.
Factores de riesgo
Los pacientes con SCR tipo 1, generalmente, son ancianos
y tienen una historia de internaciones previas por IC o por
infarto agudo de miocardio (IAM)4. Varios son los factores
asociados con disfunción cardíaca y renal17 (Tabla 1).

Tabla 1. Factores de riesgo de desarrollar síndrome
cardio-renal tipo 1
El aumento de la adiposidad está relacionado con incremento
de la secreción de citocinas como interleucina 6
(IL-6) y factor de necrosis tumoral alfa (TNF a), que
pueden estar asociados con lesión cardíaca y renal. Estas
alteraciones están asociadas a 3-7 veces de mayor riesgo
de desarrollar SCR3.
La albuminuria está relacionada con el desarrollo de IC
en aproximadamente un 30% de los pacientes y también
predispone a lesión renal aguda. En el estudio ADHERE11,
se tiene reportado, que el 20% de los pacientes con SCR
presentó elevación de los niveles de urea, y este aumento
está asociado con hipoperfusión renal secundaria a hipovolemia
o bajo debito cardíaco a pesar de la hipervolemia14.
La anemia es común en la IC y está asociada con deterioro
de la función renal y mayor morbimortalidad. Varios
son los mecanismos relacionados, como por ejemplo, la
hemodilución que bloquea el transporte normal de hierro, la inflamación que induce la deficiencia de eritropoyetina
y la caquexia5. La inflamación y aumento de citocinas que
ocurre en la IC puede causar supresión de la formación de
eritrocitos en la médula ósea. En un estudio en pacientes
con disfunción del ventrículo izquierdo (VI), se evidenció
que por cada 1% de caída del hematocrito, la tasa de
mortalidad aumentó un 2,7%17.
Fisiopatología
Varios mecanismos pueden desempeñar un papel importante
en la patogénesis de la lesión renal en el SCR agudo,
como por ejemplo, la congestión venosa, la activación
del sistema nervioso simpático (SNS) y del sistema renina
angiotensina aldosterona (SRAA), la ruptura del eje
hipotálamo hipófisis, así como la alteración de la señalización
celular inmunológica18 (Figura 2). En la IC, existe
un desequilibrio de la relación entre neuro-hormonas
vasoconstrictoras y vasodilatadoras, con predominio de
las primeras, las cuales estimulan la retención de sodio,
llevando al empeoramiento de la función renal.
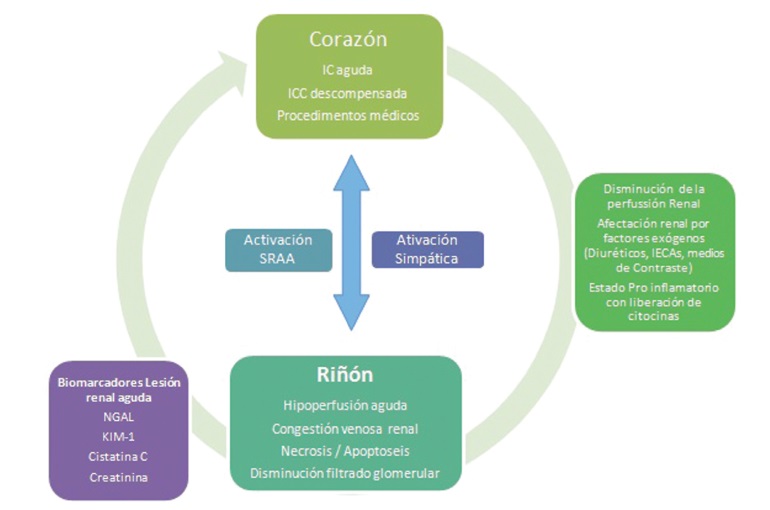
Figura 2. Fisiopatología del síndrome cardio-renal (SCR) tipo 1: relación entre insuficiencia cardíaca (IC) aguda y lesión renal.
SRAA: sistema renina-angiotensina-aldosterona. IECAs: inhibidores de la enzima convertidora de la angiotensina.
Por años se mantuvo la hipótesis de que la única causa
del SCR agudo era la hipoperfusión renal secundaria a
hipotensión o hipovolemia. En contraste, existe el hecho
de que la mayoría de los pacientes internados con SCR tipo
1 presentan síntomas y señales de volumen intravascular
aumentado, así como presiones de llenado biventricular
elevadas (clasificación de IC “caliente y húmedo”)15.
Apenas el 2,9% de los pacientes con SCR agudo se presentan
con hipotensión19, tornando al hipoflujo como una
causa poco probable de deterioro de la función renal. En
este escenario, el mecanismo autorregulador del riñón
tiene una notable capacidad para mantener su tasa de
filtración glomerular (TFG) basal adecuado, a pesar del
bajo índice cardíaco. La función renal permanece bastante
estable en la mayoría de los pacientes hipotensos con
presión arterial menor a 90 mm Hg. Por otro lado, la hipertensión
es considerada como un predictor de deterioro
de la función renal7,20.
En el estudio ADHERE11, el 50% de los pacientes que
fueron internados presentaron presión arterial sistólica
mayor o igual a 140 mm Hg. El aumento de la presión
arterial es un indicador de la retención de sodio en el
organismo y de la actividad simpática. Ventrículos con
disfunción son más sensibles a variaciones de la poscarga,
así incrementos en la presión arterial pueden empeorar
súbitamente las presiones de llenado ventricular, llevando
a congestión pulmonar independiente del volumen intravascular
total10,21.
Congestión venosa
La congestión venosa renal es una de las determinantes
hemodinámicas más importantes del SCR tipo 1. El aumento
de la presión venosa central (PVC) puede causar
elevación de la presión renal intersticial, debido a la transmisión
retrógrada de la presión auricular derecha hacia
las venas renales, que lleva a un estado de hipoxia en el
parénquima renal, teniendo como consecuencia reducción
de la excreción de sodio, que contribuye al deterioro de la
función renal en los pacientes con IC descompensada8,9.
Además, el incremento de la PVC está asociado con atenuación
de los reflejos vasculares que causa alteración de
la capacidad de respuesta vascular, perjudicando el flujo
sanguíneo renal efectivo12. Investigadores como Mullens
y col.22 incluyeron en su estudio a pacientes con IC descompensada,
de los cuales un 40% presentó aumento de
la concentración de creatinina superior o igual a 0,3 mg/
dL. Se observó que aquellos pacientes con alteración renal
tuvieron una PVC elevada antes y después de recibir
tratamiento y que el desarrollo de disfunción renal fue
infrecuente en pacientes con PVC menor a 8 mm Hg,
concluyendo que la relación entre PVC e disfunción
renal es independiente de factores como presión arterial
o índice cardíaco.
Activación neurohormonal
El sistema renina angiotensina-aldosterona tiene un
importante papel en la génesis y progresión de la IC, su
activación puede llevar a lesión renal. En la insuficiencia
cardíaca biventricular ocurre incremento precoz de la
secreción de renina, la cual estimula la liberación de
angiotensina II, aumentando la resistencia sistémica y
el tono venoso. En la IC, hay una reducción de las catecolaminas
cardíacas y aumento de las plasmáticas, esta
hiperactivación del sistema simpático está relacionada con
alteraciones de la función renal. La estimulación de los
receptores alfa en el túbulo proximal del nefrón aumenta
la reabsorción de sodio; mientras que los beta receptores
en el aparato juxtaglomerular, estimulan al SRAA. En
la IC, existe disminución de la presión pos-glomerular e
incremento de la presión oncótica, aumentando aún más
la reabsorción tubular proximal10.
La angiotensina II tiene efecto trófico directo sobre los
cardiomiocitos y células tubulares renales, promoviendo
la hipertrofia celular, apoptosis y fibrosis, además es responsable
del 50% de la liberación de aldosterona a partir
de la glándula suprarrenal, lo cual aumenta la reabsorción
renal de sodio y agua5. En individuos sanos, existe el
fenómeno de escape del efecto de la aldosterona, por el
cual la retención de sodio ocurre generalmente tres días
después, evitando la formación de edema; pero en la IC,
este fenómeno está ausente, de tal manera que la retención
de sodio es un factor que contribuye al edema y a la
congestión pulmonar6.
Sistema hipotálamo-pituitario
La arginina vasopresina es una hormona secretada en la
hipófisis posterior, su liberación es secundaria al aumento
de osmolaridad y depleción de volumen, en la IC tiene
una liberación no osmótica (citocinas). Esta hormona es
de difícil detección en sangre, ya que tiene un padrón de
secreción pulsátil e inestable; pero deriva de un precursor
peptídico a través de la copeptina, la cual es más estable
en la circulación y sus niveles en sangre son espejo de
la producción de arginina-vasopresina, por lo cual se la
considera marcador pronóstico de enfermedad aguda12.
Estimula los receptores V1a de la vasculatura y aumenta
la resistencia vascular sistémica, mientras que la estimulación
de los receptores V2 en las células del túbulo colector
causa incremento de la reabsorción de agua. También, colabora
en el transporte de urea en los túbulos colectores, lo
que lleva a un aumento de los niveles de urea nitrogenada
(BUN) en sangre17. La activación del sistema neurohormonal
causa retención de agua y sodio, congestión pulmonar
e hiponatremia. El bajo llenado arterial ocurre secundario a
la disminución del debito cardíaco en la IC de bajo débito
o vasodilatación en la IC de alto débito, teniendo como
resultado que el efecto inhibitorio de los barorreceptores
en el sistema simpático y SRAA esté atenuado, lo cual
contribuye a un círculo vicioso donde empeora la IC y la
formación de edema23.
En la IC, los péptidos natriuréticos tienen un papel importante
en la compensación de las alteraciones cardíacas en
las etapas precoces de la enfermedad; sin embargo, con la
progresión de la IC, la capacidad de los dos sistemas implicados
en la retención de sodio y agua no es suficiente2.
Inflamación e sistema de señalización celular
La IC es considerada un estado pro-inflamatorio por la
activación de citocinas en el miocardio y en los monocitos
periféricos que llevan a una transición de su fenotipo,
apoptosis y activación de metaloproteinasas de la matriz.
Las citocinas que son liberadas por leucocitos y células
tubulares renales son factores fundamentales en la patogénesis
de la lesión renal aguda24.
La caspasa es una proteína que tiene un importante papel
en el inicio de la cascada de apoptosis; cuando la célula
recibe el estimulo de apoptosis provoca la activación de
la caspasa-8 en el citoplasma, que desencadena la muerte
celular programada25. Grazia y col.18 evidenciaron en su
estudio que la actividad de la caspasa-8 fue significativamente
alta en los monocitos incubados con plasma de
pacientes con SCR tipo 1; así como también aumentaron
los niveles de IL-6 y TFN a en ellos. Estos hallazgos
sugieren que defectos en la regulación de la apoptosis de
monocitos y mecanismos inmunológicos están relacionados
con la patogénesis del SCR tipo 1.
Estrés oxidativo
La angiotensina II contribuye a la activación de la enzima
dual oxidasa, que causa formación de superóxido en las
células musculares lisas del endotelio vascular, miocitos
y células tubulares renales. Este proceso tiene consecuencias
desfavorables en los tejidos, causando inflamación y
disfunción progresiva de los órganos26. Normalmente en
respuesta al estrés oxidativo, el miocardiocito produce
grandes cantidades de péptido natriurético, que reduce la
tensión en la pared, estimula la vasodilatación y promueve
la natriuresis; mientras que en el glomérulo y túbulos
renales se produce activación del adenosin monofosfato
cíclico (AMPc), disminuyendo la retención de sodio. En
el SCR agudo, el mecanismo compensatorio está alterado,
así el paciente empeora y desarrolla oliguria a pesar de
tener niveles elevados de péptidos natriuréticos5.
Papel del intestino y la endotoxemia
La congestión venosa lleva a traslocación intestinal de
endotoxinas Gram-negativas que producen inflamación.
La liberación de citocinas en el intersticio renal causa
lesión tubular y fibrosis23. La baja perfusión intestinal
y la liberación de endotoxinas ha sido propuesto como
un mecanismo de progresión de la IC y del SCR tipo 1,
principalmente, en los pacientes con caquexia5.
En la IC, el flujo sanguíneo es desviado de la circulación
esplénica, lo que produce isquemia en las puntas de las
vellosidades. Cuando existe hipoperfusión intestinal, la
permeabilidad de la pared intestinal es incrementada por
hipoxia con producción local de lipopolisacáridos y endotoxinas
sistémicas. La afectación de la función intestinal,
la traslocación de bacterias Gram-negativas, lipopolisacáridos
y citocinas pueden exacerbar la disfunción del
miocito. La alteración del calcio intracelular del miocardio
reduce la actividad mitocondrial y provoca desequilibrio
del sistema nervioso autonómico, causando alteración
cardíaca y de otros órganos, incluyendo a los riñones5,23.
Iatrogénicas
El uso de medios de contrate para cateterismos cardíacos,
la terapia farmacológica usada para el tratamiento de la IC
como diuréticos, inhibidores de la enzima convertidora de
angiotensina y el pos-operatorio de cirugía cardíaca son
factores implicados en la aparición del SCR tipo 1 en los
días posteriores de la internación17.
Evolución y pronóstico
Un cuarto de los pacientes hospitalizados para tratamiento
de IC descompensada puede experimentar deterioro
significativo de la función renal14. La insuficiencia renal
es considerada un factor de riesgo independiente de mortalidad
a un año en los pacientes con IC aguda, siendo
también un importante marcador de pronóstico de esta enfermedad3.
En varios estudios20,27, se demostró, que en los
pacientes internados con IC descompensada, la presencia
de insuficiencia renal inicial indicaba un mal pronóstico.
El desarrollo de SCR es un marcador de progresión para
el estadio D de la IC en la clasificación de la American
Heart Association (AHA)14.
En una revisión bibliográfica sistematizada27, que incluyó 16 estudios y valoró la asociación entre alteración renal e
mortalidad en pacientes internados con IC, se consideró insuficiencia renal moderada a severa cuando los valores
de creatinina fueron mayores o iguales a 1,5 mg/dL o la
tasa de filtración glomerular (TFG) menor a 53 ml/min,
como resultado se reportó que el riesgo de mortalidad
aumentó un 15% por cada 0,50 mg/dL de incremento de
creatinina y un 7% por cada 10 ml/min de disminución de
TFG. La TFG se asoció con aumento del riesgo de eventos
cardiovasculares20.
Testani y col.29 evidenciaron que la hemoconcentración
está asociada con el deterioro de la función renal; pero
también, fue relacionada con una tasa de mortalidad
menor, sugiriendo que el descongestionamiento agresivo
con diuréticos, a pesar del deterioro de la función renal
en etapas precoces puede tener un efecto favorable en la
sobrevida de estos pacientes.
Niveles de nitrógeno ureico en sangre (BUN) mayores a
50 mg/dL fueron identificados como un mejor predictor de
mortalidad intrahospitalaria en pacientes con IC descompensada11.
Niveles aumentados de arginina-vasopresina
están asociados con activación de SRAA y SNS, considerados
importantes predictores de mortalidad. Pacientes
con IC que presentan niveles de péptido natriurético tipo
B (BNP) de 480 pg/mL tienen una probabilidad de un
51% de muerte y reinternación hospitalaria17. También la
hiponatremia, que es común en pacientes con IC, está asociada
con alta morbilidad en los pacientes con IC crónica.
Papel de los nuevos biomarcadores en el SCR tipo 1
El uso de biomarcadores como péptidos natriuréticos,
troponinas y marcadores renales ayudan en la predicción
de riesgo y en el pronóstico de la IC30,31,40. El BNP y el
NT-proBNP son importantes para informar diagnóstico
y pronóstico de pacientes con alteraciones en el corazón
y riñón. Varios estudios retrospectivos27,32 han reportado
una asociación del SCR tipo 1 con internación hospitalaria
prolongada y mal pronóstico; así, la identificación precoz
de estos pacientes puede representar una oportunidad
para implementar estrategias que ayuden a prevenir la
alteración de la función renal.
La creatinina sérica no es un método adecuado para
identificar modificaciones agudas de la función renal.
Por este motivo, el papel de los biomarcadores como la
lipocalina asociada a gelatinasa de neutrófilos (NGAL),
la molécula de injuria renal 1 (KIM-1), la N-acetil-b-Dglucosaminidasa
(NAG) y la cistatina C, están siendo
investigadas para valorar su utilidad en la detección de
lesión renal aguda3 (Figura 3).
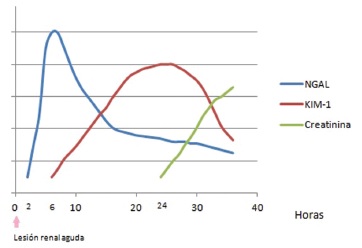
Figura 3. Detección de los niveles de biomarcadores de lesión
renal: se observa que los niveles de NGAL y KIM-1 pueden ser
detectados en forma precoz aproximadamente 24 a 48 horas antes
del aumento de creatinina en sangre.
NGAL: lipocalina asociada a gelatinasa de neutrófilos. KIM-1:
molécula de injuria renal 1.
La cistatina C es un inhibidor de la proteasa de cisteína, la
cual es sintetizada por células nucleadas que son filtradas
en el glomérulo y reabsorbidas en el túbulo proximal. En
pacientes con índices de masa corporal extrema, indica
la TFG verdadera, ya que no es afectada por la masa
muscular. Sus niveles en sangre son detectados precozmente
antes que los niveles de creatinina, por lo cual es
considerada un buen marcador de lesión renal precoz33.
Lassus y col.16 evidenciaron en su estudio que el aumento
de los niveles de cistatina C mayor o igual a 0,3 mg/L
fue asociado con alta mortalidad intrahospitalaria, razón
por la cual la cistatina C es considerada como un potente
marcador de detección de lesión renal aguda precoz y de
pronóstico en el SCR agudo. Un inconveniente es su costo.
La NGAL es una glicoproteína que pertenece a la superfamilia
de las lipocalinas, sintetizada en la médula ósea
durante la maduración de los granulocitos y liberado por
neutrófilos y células epiteliales que incluyen a las células
renales del túbulo proximal33. Los niveles de NGAL en
sangre y orina están significativamente elevados en pacientes
con lesión renal aguda, este aumento ocurre 24 a 48
horas antes del incremento de creatinina plasmática32. En
un metanalisis25 se reportó que el incremento de NGAL
identifico el 40% de los casos de IC asociada a lesión renal.
Alvelos y col.32 en su estudio sugieren que NGAL puede
ser una fuerte herramienta auxiliar en el reconocimiento
precoz de los pacientes con IC aguda que desarrollaran
SCR; así, la NGAL es un predictor independiente de
desarrollo de SCR tipo 1, por cada 10 mg/L de aumento
de los niveles de NGAL hay un 31% de riesgo adicional
de disfunción renal. NGAL, también, ha sido valorada
como biomarcador de lesión renal en adultos que van a
ser sometidos a cirugía cardíaca y en la nefropatía inducida
por contraste34. NGAL combinada con el BNP son
probablemente los marcadores que han presentado más
evidencia de éxito en el diagnóstico del SCR tipo 1. El
BNP aporta precozmente datos de presencia de sobrecarga
de volumen y la NGAL indica lesión renal precoz6.
Niveles plasmáticos de NGAL aumentan con enfermedades
inflamatorias, siendo menos específica que los niveles
de NGAL urinario. Haase y col.36 en su estudio evidenciaron
que la cuantificación de NGAL urinario fue superior
como predictor de lesión renal aguda que la NGAL sérica.
La molécula de lesión renal 1 (KIM-1) es un tipo de
proteína transmembrana detectable 24 horas antes de la
elevación de los niveles de creatinina sérica. Su liberación
ocurre después de isquemia o nefrotoxicidad de las células
del túbulo renal proximal. Junto con la NGAL son marcadores importantes en la etapa inicial de la lesión renal16,34.
La NAG es una enzima lisosomal, liberada por las células
tubulares renales cuando existe lesión, por lo cual es
considerado un excelente predictor de lesión renal aguda.
Niveles elevados de NAG han sido encontrados en los
pacientes con IC con TFG levemente reducida34.
Tratamiento
En el tratamiento del SCR tipo 1, las estrategias para mejorar el debito cardíaco y la presión de perfusión renal son importantes, evidencias recientes sobre la patogénesis del síndrome cardio-renal, que incluyen mecanismos como elevada presión venosa, aumento de la presión intraabdominal y congestión renal, indican la utilidad de diuréticos y vasodilatadores en el tratamiento precoz35. Los SCR tipo 1 y 2 tienen componentes reversibles, de tal manera que una mejor función cardíaca puede producir aumento de la TFG.
Diuréticos
Reducen rápidamente la presión de llenado ventricular y
la congestión pulmonar17. Los diuréticos de asa producen
diuresis y alivio de los síntomas de congestión; pero también,
provocan una acentuada activación del SNS y del
SRAA, por lo cual puede ser considerado precipitantes
del SCR agudo5,15.
En el SCR, existe una respuesta disminuida a los diuréticos
debido al fenómeno de frenado diurético, que consiste en
la retención de sodio después de una dosis de diurético5.
Los mecanismos propuestos para explicar la resistencia a
los diuréticos incluyen: disminución de la TFG, activación
del SRAA e hipertrofia de las células epiteliales del túbulo
distal17. Para evitar este fenómeno, se puede usar una dosis
intravenosa continua o añadir otro diurético que bloquee
el efecto en el túbulo distal.
El uso de diuréticos de asa en los pacientes con IC predispone
a alteraciones electrolíticas e hipovolemia, que lleva
a la activación neuro-hormonal y lesión renal aguda4. En la
IC, los niveles elevados de adenosina pueden disminuir la
TFG por vasodilatación de los capilares pos-glomerulares
y vasoconstricción de la arteria eferente; además, la
estimulación de los receptores adenosina A1 aumenta
la reabsorción de sodio y agua en el túbulo proximal y
distal. El aumento de la excreción de sodio por la terapia
diurética estimula la liberación de adenosina por retroalimentación
en la mácula densa y arteriola eferente con
reducción de la TFG14.
Sin embargo, varios estudios evidenciaron11,15 que a pesar
del deterioro de la función renal, la infusión intravenosa
de furosemida resultó eficaz en la mejora hemodinámica
y sintomática de la IC; así como, la función renal también
se normalizó. Estos resultados apoyan la conclusión de
que el síndrome cardio-renal es un estado de hipervolemia
con flujo normal.
Los diuréticos son frecuentemente utilizados en dosis
sub-terapéutica e interrumpidos prematuramente antes
de alcanzar la mejoría hemodinámica o euvolemia.
Aproximadamente, el 50% de los pacientes con IC descompensada
tienen el alta hospitalaria sin conseguir las
metas de reducción de peso corporal, lo cual puede llevar
a presiones de llenado crónicas elevadas y incremento de
las tasas de re-internación.
El análisis de bioimpedancia vectorial (BIVA) es un método
no invasivo que estima los niveles de agua corporal
total, usando una corriente eléctrica alterna que pasa a través
del tejido biológico, valorando la hidratación corporal
por resistencia y reactancia. Tanto el uso de BIVA como
de biomarcadores como el BNP podrían ayudar para un
mejor control de los diuréticos en pacientes en tratamiento
de IC descompensada6.
Conclusión
El síndrome cardio-renal tipo 1 es un conjunto de procesos
fisiopatológicos que contribuyen a la perpetuación de un
círculo vicioso de disfunción cardíaca y renal. Es frecuente
en pacientes con IC descompensada, está asociado con mal
pronóstico y mayores tasas de re-internación hospitalaria,
por lo cual, precisa de un abordaje rápido, cuidadoso e
multidisciplinar. NGAL y KIM-1 son nuevos biomarcadores
descubiertos, detectados precozmente, incluso antes
que los niveles de creatinina sérica comiencen a elevarse,
identificando pacientes cardíacos que están en riesgo de
desarrollar lesión renal aguda.
El manejo del SCR agudo es un desafío, debido a las
limitaciones impuestas por la lesión renal aguda en la
capacidad de corregir la sobrecarga de volumen, en los últimos años se está dando mayor importancia al estudio
de las interacciones existentes entre el corazón y el riñón,
con la finalidad de encontrar estrategias que ayuden en la
prevención de alteraciones renales en pacientes con IC.
Recursos financieros
Los autores no recibieron ningún apoyo económico para la investigación.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
1. Go AS, Mozaffarian D, Roger VL, Benjamin EJ, Berry JD, Blaha MJ, et al. Heart disease and stroke statistics-2014 update: a report from the American Heart Association. Circulation 2014;129: e28-e292.
2. Boerrigter G, Burnett J. Cardiorenal Syndrome in Decompensated Heart Failure: Prognostic and Therapeutic Implications. Curr Heart Fail Rep 2004;1: 113-120.
3. Ronco C, Haapio M, House A, Anavekar N, Bellomo R. Cardiorenal Syndrome. J Am Coll Cardiol 2008;52: 1527-39.
4. Cruz D. Cardiorenal Syndrome in Critical Care: The Acute Cardiorenal and Renocardiac Syndromes. Adv Chronic Kidney Dis 2013; 20, (1): 56-66.
5. Ronco C, Cicoira M, McCullough PA. Cardiorenal Syndrome Type 1. Pathophysiological Crosstalk Leading to Combined Heart and Kidney Dysfunction in the Setting of Acutely Decompensated Heart Failure. J Am Coll Cardiol 2012;60: 1031-42.
6. Ronco C, Kaushik M, Valle R, Aspromonte N, Peacock IV WF. Diagnosis and Management of Fluid Overload in Heart Failure and Cardio-Renal Syndrome: The “5B” Approach. Semin Nephrol 2012; 32: 129-141.
7. Ljungman S, Laragh JH, Cody RJ. Role of the kidney in congestive heart failure: Relationship of cardiac index to kidney function. Drugs 1990; 39(Suppl 4): 10-21.
8. Metra M, Cotter G, Gheorghiade M, Dei Cas L, Voors A. The role of the kidney in heart failure. Eur Heart J 2012;33(17): 2135-42.
9. Graziani G, Pini D, Oldani S, Cucchiari D, Podesta MA, Badalamenti S. Renal dysfunction in acute congestive heart failure a common problem for cardiologists and nephrologists. Heart Fail Rev 2014;19(6): 699-708.
10. Haase M, Müller C, Damman K, Murray PT, Kellum JA, Ronco C, et al. Pathogenesis of Cardiorenal Syndrome Type 1 in Acute Decompensated Heart Failure: Workgroup Statements from the Eleventh Consensus Conference of the Acute Dialysis Quality Initiative (ADQI). Contrib Nephrol 2013;182: 99-116.
11. Fonarow GC, Adams KF, Abraham WT, Yancy CW, Boscardin WJ; ADHERE Scientific Advisory Committee. Risk stratification for inhospital mortality in acutely decompensated heart failure: Classification and regression analysis. JAMA 2005; 293: 572-580.
12. Udani S, Koyner JL. The Effects of Heart Failure on Renal Function. Cardiol Clin 2010;28(3): 453-65.
13. Gottlieb SS, Abraham W, Butler J, et al. The prognostic importance of different definitions of worsening renal function in congestive heart failure. J Card Fail 2002;8: 136-141.
14. Liang KV, Williams AW, Greene EL, Redfield MM. Acute decompensated heart failure and the cardiorenal syndrome. Crit Care Med 2008; 36: S75-S88.
15. Wencker D. Acute Cardio-renal Syndrome: Progression from Congestive Heart Failure to Congestive Kidney Failure. Curr Heart Fail Rep 2007;4(3): 134-8.
16. Lassus JP, Nieminen MS, Peuhkurinen K, Pulkki K, Siirila-Waris K, Sund R, et al. Markers of renal function and acute kidney injury in acute heart failure: definitions and impact on outcomes of the cardiorenal syndrome. Eur Heart J 2010;31(22): 2791-8.
17. Sarraf M, Masoumi A, Schrier RW. Cardiorenal Syndrome in Acute Decompensated Heart Failure. Clin J Am Soc Nephrol 2009; 4: 2013-2026.
18. Grazia M, Torregrossa R, Cruz D, Chionh CY, De Cal M, Soni S, et al. Cardiorenal Syndrome Type 1 May Be Immunologically Mediated: A Pilot Evaluation of Monocyte Apoptosis. Cardiorenal Med 2012;2: 33-42.
19. Heywood JT. The cardiorenal syndrome: lessons from the ADHERE database and treatment options. Heart Fail Ver 2004;9:195-201.
20. Nohria A, Hasselblad V, Stebbins A, Pauly DF, Fonarow GC, Shah M, et al. Cardiorenal interactions: insights from the ESCAPE trial. J Am Coll Cardiol 2008;51(13): 1268-74.
21. Forman DE, Butler J, Wang Y, et al. Incidence, predictors at admission, and impact of worsening renal function among patients hospitalized with heart failure. J Am Coll Cardiol 2004;43: 61-7.
22. Mullens W, Abrahams Z, Francis GS, Sokos G, Taylor DO, Starling RC, et al. Importance of venous congestion for worsening of renal function in advanced decompensated heart failure. J Am Coll Cardiol 2009;53: 589-96.
23. Cole RT, Masoumi A, Triposkiadis F, Giamouzis G, Georgiopoulou V, Kalogeropoulos A, et al. Renal Dysfunction in Heart Failure. Med Clin North Am 2012;96(5): 955-74.
24. Lee DW, Faubel S, Edelstein CL. Cytokines in acute kidney injury (AKI). Clin Nephrol 2011; 76: 165-173.
25. Haase M, Devarajan P, Haase-Fielitz A, Bellomo R, Cruz DN, Wagner G. The Outcome of Neutrophil Gelatinase-Associated Lipocalin-Positive Subclinical Acute Kidney Injury. J Am Coll Cardiol 2011; 57: 1752-61.
26. Casado J, Perez JI. Daño orgánico y síndrome cardiorrenal en la insuficiencia cardíaca aguda. Med Clin Barc 2014;142 Suppl 1: 26-31.
27. Virzi MG, Clemente A, De Gal M, Brocca A, Day S, Pastori S, Bolin Chiara, Vescovo G, Ronco C. Oxidative stress: dual pathway induction in cardiorenal syndrome type 1 pathogenesis. Oxid Med Cell Longev 2015; pag: 1-9.
28. Smith GL, Lichtman JH, Bracken MB, et al. Renal impairment and outcomes in heart failure: Systematic review and metaanalysis. J Am Coll Cardiol 2006; 47: 1987-1996.
29. Testani JM, Chen J, McCauley BD, Kimmel S, Shannon R. Potential Effects of Aggressive Decongestion During the Treatment of Decompensated Heart Failure on Renal Function and Survival. Circulation 2010;122: 265-272.
30. Cruz DN, Fard A, Clementi A, Ronco C, Maisel A. Role of biomarkers in the diagnosis and management of cardio-renal syndromes. Semin Nephrol 2012;32: 79-92.
31. Kshatriya S, Kozman H, Siddiqui D, Bhatta L, Liu K, Salah A, et al. El síndrome cardio-renal en insuficiencia cardíaca: Un paradigma en evolución. Rev Chil Cardiol 2011; 31: 160-167.
32. Alvelos M, Pimentel R, Pinho E, Gomes A, Lourenço P¸ Teles MJ, Almeida P, et al. Neutrophil Gelatinase-Associated Lipocalin in the Diagnosis of Type 1 Cardio-Renal Syndrome in the General Ward. Clin J Am Soc Nephro 2011; 6: 476-481.
33. Tan K, Sethi S. Biomarkers in cardiorenal syndromes. Transl Res 2014;164(2): 122-34.
34. Taub P, Borden K, Maisel A. Role of biomarkers in the diagnosis and prognosis of acute kidney injury in patients with cardiorenal syndrome. Expert Rev Cardiovasc Ther 2012; 10(5): 657-667.
35. House AA, Haapio M, Lassus J, Bellomo R, Ronco C. Therapeutic strategies for heart failure in cardiorenal syndromes. Am J Kidney Dis2010;56(4): 759-73.
36. Haase M, Bellomo R, Devarajan P, Schlattmann P, Haase-Fielitz A, NGAL Meta-analysis Investigator Group. Accuracy of neutrophil gelatinase-associated lipocalin (NGAL) in diagnosis and prognosis in acute kidney injury: a systematic review and meta-analysis. Am J Kidney Dis 2009;54: 1012-24.